 2025-12
2025-12摘要:氧化降解是影响药物制剂稳定性、安全性和有效性的关键因素。从药物制剂研发与生产的全链条视角,系统性综述了氧化杂质的产生根源,涵盖原料药(API)、辅料、包装材料、生产设备及制药用水等关键环节。分析了各环节诱导氧化的机制,并基于质量源于设计(QbD)理念,提出了一系列切实可行的预防与控制策略,旨在为药物研发和生产过程建立完善的氧化杂质控制体系提供科学参考。
关键词:氧化杂质;药物稳定性;降解机理;原辅料相容性;包装系统;生产工艺控制;质量源于设计。
1. 引言
在药物制剂的整个生命周期中,活性药物成分(API)可能发生多种化学降解反应,其中氧化反应因其普遍性和复杂性而成为最具挑战性的降解途径之一。氧化杂质不仅可能降低产品的效价,更可能引入具有潜在毒性的杂质,直接影响用药安全。因此,对氧化杂质的深入研究与有效控制是药物分析、制剂开发及生产质量管理的核心任务。氧化反应的发生并非孤立事件,而是API与所处微环境(包括处方组分、包装系统、生产工艺环境等)相互作用的结果。本文旨在构建一个系统性的分析框架,全面剖析制剂中氧化杂质的来源,并提出综合性的控制方案。
2. 氧化杂质的来源与形成机制分析
2.1 原料药(API)的内在属性
API的化学结构是决定其氧化敏感性的根本因素。易被氧化的官能团包括:
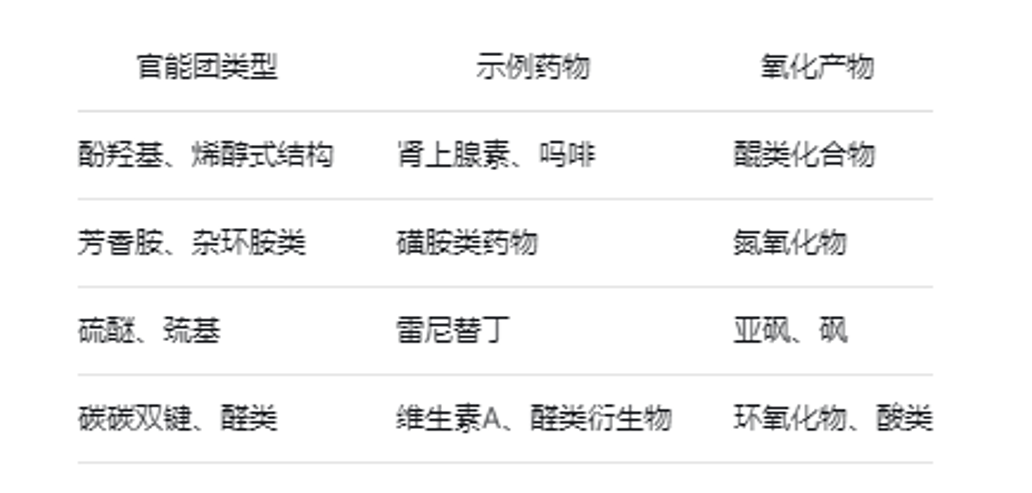
此外,API中残留的微量过渡金属离子(如Fe²⁺、Cu²⁺、Mn²⁺)是强有力的氧化反应催化剂,可显著加速自由基引发的自氧化过程。
2.2 辅料的影响
辅料远非“惰性”,其可能通过多种途径引入氧化风险:
· 氧化性杂质:某些辅料(如聚乙二醇PEG、聚乙烯吡咯烷酮PVP、某些表面活性剂)在生产过程中可能引入过氧化物、过氧化物等残留杂质,成为直接的氧化剂。
· 水分:亲水性辅料(如乳糖、微晶纤维素)的吸湿性可能增加体系中的水分活度,水分既可作为反应介质,也可能参与水解-氧化耦合反应。
· 金属离子:部分矿物质来源的辅料(如磷酸氢钙、二氧化钛)可能携带催化性金属杂质。
· pH调节作用:辅料或pH调节剂可能改变制剂的微环境pH,影响某些氧化反应的速率(如胺类在特定pH下更易氧化)。
2.3 包装系统的影响
包装系统是制剂抵御外界氧化威胁的第一道防线,其本身也可能成为污染源:
· 氧气透过:塑料容器、泡罩包装(尤其是PVC)对氧气有一定的透过率,是贮存期间氧气的主要来源。橡胶塞同样具有透气性。
· 浸出物:橡胶塞中的硫化剂、抗氧化剂、填料,塑料容器中的单体、增塑剂、抗氧化剂等可能浸出至药液中,部分浸出物可能具有氧化性或催化氧化作用。
· 密封性:包装系统密封不严会导致氧气持续渗入。
2.4 生产设备与工艺过程
生产过程中的诸多环节可能引入氧化应激:
· 混合与制粒:高速剪切、长时间混合使物料与空气充分接触,并可能产热。
· 干燥与灭菌:高温过程(如流化床干燥、终端灭菌)显著加速氧化反应动力学。
· 设备接触:设备表面(特别是磨损部位)的金属颗粒(不锈钢中的铁、铬、镍)可能脱落进入产品,成为催化中心。清洁残留的氧化性消毒剂(如过氧乙酸、次氯酸钠)是高风险源。
· 充氮保护失效:在关键工艺步骤(如灌装、压塞)中,惰性气体(氮气/氩气)保护不充分或气体纯度不够,无法有效置换顶空氧。
2.5 制药用水
制药用水(纯化水、注射用水)是液体制剂、湿法制粒的主要溶剂,其质量至关重要:
· 溶解氧:水中溶解的氧气是直接的氧化剂来源。水温升高、湍流搅拌会降低氧溶解度但增加传质速率。
· 氧化性无机物:如残留氯(来自市政供水消毒)、臭氧、过氧化氢(可能来自水系统消毒)。
· 微生物与内毒素:微生物代谢可能产生具有氧化性的副产物。
3. 综合控制策略与解决措施
基于上述根源分析,控制氧化杂质需采取多层次、前瞻性的综合策略。
3.1 处方前研究与处方设计
3.1.1API筛选与修饰
在早期开发中,评估API的氧化敏感性,必要时考虑成盐、酯化或使用更稳定的晶型。
3.1.2辅料精选与相容性研究
建立辅料氧化性杂质(特别是过氧化物)的检测标准,优先选择低氧含量、低金属杂质、低过氧化值的辅料供应商。
进行强制降解条件下的原辅料相容性试验,评估不同辅料对API氧化稳定性的影响。
3.1.3 添加稳定剂
抗氧化剂:根据药物性质选择合适的抗氧剂(如水溶性:亚硫酸盐、抗坏血酸、硫代硫酸钠;油溶性:生育酚、没食子酸酯、BHT/BHA)。需注意抗氧剂与API的相容性及自身毒性。
金属螯合剂:添加EDTA、枸橼酸等,有效络合催化性金属离子,阻断金属催化氧化路径。
3.1.4优化pH
通过缓冲体系将制剂调节至API氧化速率最低的稳定pH范围。
3.2包装系统筛选与验证
3.2.1阻隔性评估
根据产品敏感性,选择具有高氧气阻隔性的包装材料,如玻璃安瓿、铝塑复合膜泡罩、COP/COC聚合物瓶、覆盖有聚四氟乙烯膜的橡胶塞等。
3.2.2相容性研究
按照ICH Q1A和《化学药品注射剂与塑料包装材料相容性研究技术指导原则》等,对包装材料进行提取研究、相互作用研究(迁移与吸附)和安全性评估。
3.2.3密封完整性测试
在生产开始和结束时,采用物理或微生物挑战法验证包装的密封性。
3.3生产工艺的优化与控制
3.3.1 建立低氧生产工艺
在溶解、混合、灌装等关键工序实施充氮保护,并对氮气纯度和流量进行在线监测与控制。对药液进行脱氧处理(如通氮鼓泡、真空脱气)。
3.3.2 控制温度与光照
明确对光敏感产品的避光操作要求,严格控制对热敏感工序的暴露时间和温度。
3.3.3设备管理与清洁验证
选用耐腐蚀、高光洁度的设备(如316L不锈钢),定期检查维护,防止金属颗粒脱落。制定严格的清洁规程,确保有效去除氧化性清洁剂残留,并在清洁后验证其残留量。
3.3.4过程分析技术(PAT)应用
考虑在线监测关键工艺参数(如溶解氧含量、顶空氧浓度),实现实时质量控制。
3.4制药用水系统的控制
· 定期监测与维护:除常规化学和微生物指标外,建立关键用水点溶解氧的监测警戒限和行动限。对水系统进行定期消毒,并验证消毒剂的有效清除。
· 使用点处理:对于高风险产品,可在使用点安装惰性气体喷射或脱氧装置,进一步降低用水的氧含量。
3.5 全面的分析方法与稳定性研究
· 开发灵敏、专属的分析方法:采用HPLC-DAD/FLR、LC-MS/MS等手段,对氧化降解产物进行鉴定、定量,建立合理的控制策略(如根据ICH Q3A/B设定制剂杂质的报告阈、鉴定阈和界定阈)。
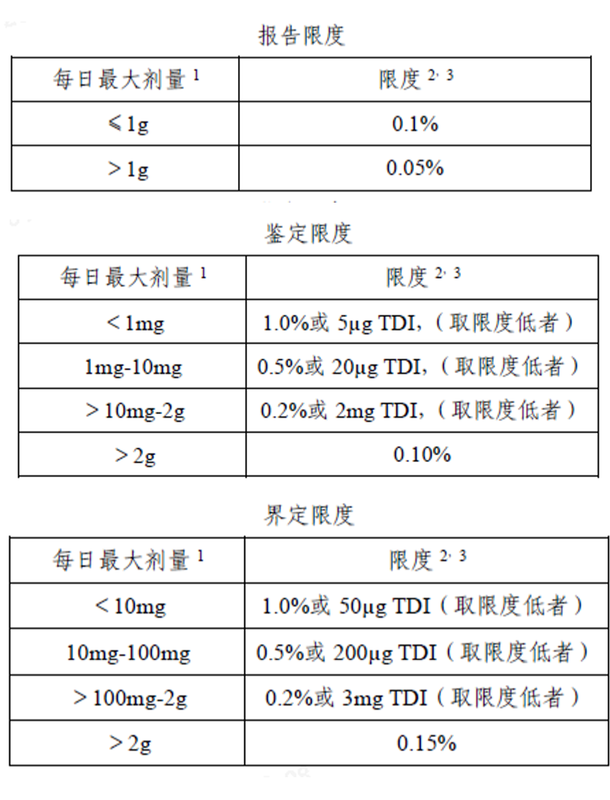
· 科学的稳定性研究设计:在影响因素试验中系统考察氧、光、热、湿等因素的影响。在加速和长期稳定性试验中,使用与实际生产相同的包装,并在稳定性考察点监测氧化杂质的变化趋势。考虑进行包装在半满状态下的稳定性研究,以评估顶空氧的影响。
4. 结论
药物制剂中氧化杂质的控制是一项贯穿于研发、生产、储存全过程的系统工程。它要求药物分析人员与制剂研发、生产、包装工程及质量管理团队紧密协作,基于对API理化性质的深刻理解,运用质量源于设计(QbD)的理念,从原辅料控制、处方设计、包装筛选、生产工艺优化到全程质量监测,构建一个多维度的、主动的防御体系。唯有通过这种系统性的研究和前瞻性的控制,才能确保药物产品在整个货架期内的质量、安全性和有效性,最终保障患者的用药安全。
参考文献
[1] ICH Q1A(R2): Stability Testing of New Drug Substances and Products.
[2] ICH Q3B(R2): Impurities in New Drug Products.
[3] 《化学药品注射剂与药用玻璃包装容器相容性研究技术指导原则》.
[4] Waterman, K. C., et al. (2002). Hydrolysis in Pharmaceutical Formulations. Pharmaceutical Research, 19(3), 288-295.
[5] Reed, R. A., et al. (2016). Oxidation of Pharmaceuticals: Theory and Practice. Wiley.








